Τα (υποθετικά προς το παρόν) στοιχεία του περιοδικού πίνακα με ατομικούς αριθμούς Ζ=119 και Ζ=120, ονομάζονται αντίστοιχα: Ουνουνέννιο (119Uue) ή Eκα-φρανκιο και Ουνμπινίλιο (120Ubn) ή Εκα-ράδιο.
Τα προθέματα eka- , μαζί με τα dvi- και tri- , χρησιμοποιούνταν από τον Mendeleev (από τα σανσκριτικά ονόματα των ψηφίων 1, 2 και 3), για την προσωρινή ονομασία στοιχείων που δεν είχαν ανακαλυφθεί. Για παράδειγμα στην σημερινή ομάδα του Βορίου (Ζ=5), ο Mendeleev προέβλεψε ότι υπήρχε ένα έως τότε άγνωστο στοιχείο, αμέσως μετά το Αλουμίνιο (Ζ=13), που το ονόμασε Εκα-αλουμίνιο, προβλέποντας ότι το ατομικό του βάρος θα είναι 68. Το στοιχείο αυτό ανακαλύφθηκε αργότερα και ονομάστηκε Γάλλιο (Ζ=31).
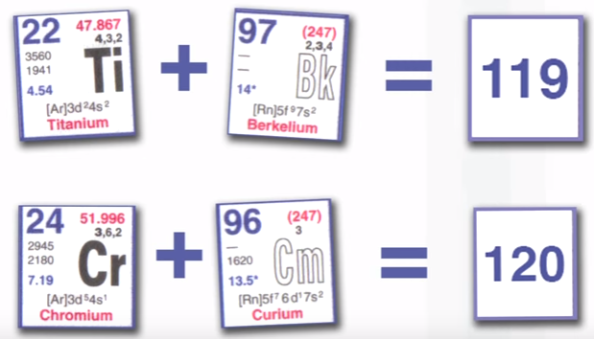
Στο Ινστιτούτο Πυρηνικών Ερευνών της Ντούμπνα στην Ρωσία προγραμματίζονται νέα πειράματα δημιουργίας του Ουνουνένιου και του Ουνμπινίλιου, διαμέσου των πυρηνικών αντιδράσεων σύντηξης όπως 249Bk+50Ti και 249Cf+50Ti ή 96Cm + 24Cr, αντίστοιχα.
Στο βίντεο που ακολουθεί ο καθηγητής Martyn Poliakoff μας παρουσιάζει τις προσπάθειες δημιουργίας αυτών των υπερ-βαρέων στοιχείων:
Στο βίντεο που ακολουθεί ο καθηγητής Martyn Poliakoff μας παρουσιάζει τις προσπάθειες δημιουργίας αυτών των υπερ-βαρέων στοιχείων:
Μπορείτε επίσης να δείτε σχετική αναφορά και ΕΔΩ









